
Durch die Substitution (Ersatz) im Fischfutter von Fischmehl durch pflanzliche Inhaltsstoffe, können in Pflanzen verbliebene Pestizidrückstände ins Fischfutter und damit in den Fisch gelangen. Foto: Pixabay
Auf einen Blick: Endosulfan
Endosulfan ist ein effektives und preisgünstiges neurotoxisches Insektizid und Akarizid. In der EU und vielen weiteren Ländern ist der Einsatz von Endosulfan verboten. Durch die Substitution (Ersatz) im Fischfutter von Fischmehl durch pflanzliche Inhaltsstoffe, können in Pflanzen verbliebene Pestizidrückstände ins Fischfutter und damit in den Fisch gelangen. Eine potentielle Gefährdung durch Anreicherung von Endosulfan in Fischprodukten ist als gering einzustufen.
Detaillierte Informationen finden Sie im Hauptartikel.
_______________________
Endosulfan wurde in den 1950er-Jahren entwickelt und in den folgenden Jahrzehnten weltweit als effektives und preisgünstiges Insektizid und Akarizid in der Land- und Forstwirtschaft sowie zur Bekämpfung krankheitsübertragender Insekten wie der Tsetse-Fliege (Schlafkrankheit – Trypanosomiasis) und als Holzschutzmittel eingesetzt.
Die genaue Bezeichnung für Endosulfan gemäß der Nomenklatur lautet:
6,7,8,9,10,10-Hexachlor-1,5,5a,6,9,9a-hexahydro-6,9-methano-2,4,3-benzo-dioxathiepin-3-oxid
Es trägt die CAS-Nummer 115-29-7.
Das als Pestizid eingesetzte Produkt besteht aus den Diastereomeren α- und β-Endosulfan im Verhältnis von 64:36. Es besitzt eine hohe akute Toxizität gegenüber Wirbeltieren und kann als endokriner Disruptor das Hormonsystem (z. B. Steroidogenese) beeinträchtigen und beispielsweise die Reproduktion beeinflussen. Endosulfan ist, wie alle anderen Chlorpestizide auch, chemisch ausgesprochen stabil und wird daher in der Umwelt nur sehr langsam abgebaut.
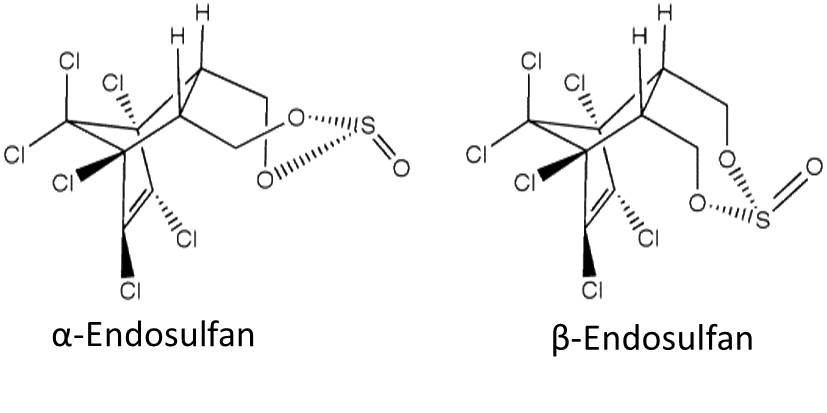
Seine hohe Persistenz, eine Tendenz zur Bioakkumulation und die damit einhergehende Gefährdung für Mensch und Umwelt haben dazu geführt, dass der Einsatz von Endosulfan mittlerweile in über 80 Ländern verboten ist. In Deutschland wurde Endosulfan bereits 1991 die Zulassung entzogen (in den neuen Bundesländern 1994). EU-weit wurde der Einsatz von Endosulfan erst 2005 verboten. Im April 2011 wurde Endosulfan schließlich in die POP-Liste (POP = Persistente organische Schadstoffe) der Stockholm-Konvention aufgenommen und damit ein weltweites Herstellungs- und Anwendungsverbot verhängt. Allerdings tritt dieser Beschluss landesabhängig mit z. T. langjährigen Übergangsfristen (max. 10 Jahre) in Kraft.
Wirkungsweise
Endosulfan ist ein sehr effektives Neurotoxin, das in Insekten die γ-Aminobuttersäure (GABA)-gesteuerten Chloridkanäle blockiert und so die neuronale Erregungsleitung stört.
GABA wird von bestimmten Nervenzellen als Neurotransmitter in den Synapsenspalt ausgeschüttet und bewirkt in der nachgeschalteten Nervenzelle die Öffnung von Chloridkanälen. Die verstärkt in das Zellinnere einströmenden negativ geladenen Chloridionen erniedrigen das bestehende Membranpotential und erhöhen somit den Schwellenwert, der für die Auslösung eines Aktionspotentials nötig ist (Erregungsleitung).
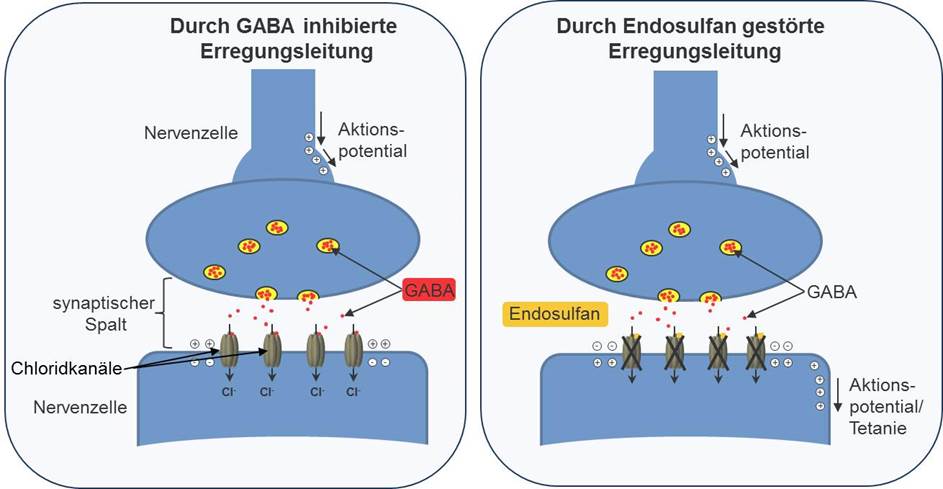
Die Nervenzelle ist folglich schwerer erregbar. Endosulfan unterbindet die regulierende Funktion von GABA, indem es an den GABA-Rezeptor bindet und diesen blockiert. Durch den Wegfall der inhibitorischen Wirkung von GABA wird die Erregungsleitung gestört, was in den betroffenen Insekten zu Dauererregungen der nachgeschalteten Muskel- und Nervenzellen führt. Neben der Blockade der Chloridkanäle werden auch verschiedene ATPasen (NA+/K-, Ca2+, Mg+) in ihrer Funktion beeinträchtigt. Dies führt ebenfalls zu einer Beeinträchtigung elektrophysiologischer Prozesse und zahlreicher metabolischer Prozesse, wie z. B. der osmotischen Regulation oder des Lipidstoffwechsels.
Vorkommen in der Umwelt

Durch seine hohe Persistenz (Bestehenbleiben eines Zustands über längere Zeit) ist Endosulfan nicht nur im Ackerboden und den meisten Gewässern und Meeren nachweisbar, sondern auch in der Luft. Nennenswerte Mengen wurden ebenfalls in Bereichen gefunden, die weitab menschlicher Nutzung liegen, wie z. B. der Arktis. Wenn auch Endosulfan als POP sehr beständig ist, wird es doch im Laufe der Zeit durch biotische (mikrobieller Abbau) und abiotische (z. B. Hydrolyse) Prozesse zumeist in das 10-fach weniger toxische Endosulfansulfat degradiert. Die Geschwindigkeit der Abbauprozesse hängt dabei von einer Vielzahl von Faktoren ab (Temperatur, Sauerstoffgehalt, chemisches Isomer und ob das Endosulfan im Bodengrund gebunden, im Wasserkörper gelöst oder in der Luft vorliegt).
Endosulfan in Produkten aus der Aquakultur
Da in der modernen Aquakultur vermehrt Fischmehl und Fischöl durch pflanzliche Substitutionsstoffe ersetzt werden, können in Pflanzen verbliebene Pestizidrückstände ins Fischfutter und damit in den Fisch gelangen. Besonders die nur noch sehr selten eingesetzten bzw. mittlerweile verbotenen Chlorpestizide, wie DDT, Lindan oder auch Endosulfan, sind sehr persistent und können sich so im Fisch anreichern.
Obwohl Endosulfan 2011 in die Liste der POP aufgenommen wurde (weltweites Herstellungs- und Anwendungsverbot), hat die EU den bis 2013 geltenden Grenzwert für Endosulfan in Salmonidenfutter von 0,005 mg/kg auf 0,05 mg/kg heraufgesetzt. Der geltende Grenzwert für Rückstände im Fisch selbst blieb unangetastet bei maximal 0,1 mg/kg. Da der von der FAO (engl. Food and Agriculture Organisation of the United Nations, Ernährungs- und Landwirtschaftsorganisation der Vereinten Nationen) und der WHO (engl. World Health Organisation, Weltgesundheitsorganisation) definierte ADI (engl. Acceptable Daily Intake – beziffert die tägliche Aufnahmemenge von Fremdstoffen in Lebensmitteln, die ein Mensch lebenslänglich pro Tag verzehren kann, ohne gesundheitliche Schäden davonzutragen) 0,006 mg/kg Endosulfan pro Tag beträgt, müsste ein 70 kg schwerer Erwachsener dementsprechend mehr als 4 kg Fisch pro Tag verzehren, der mit 0,1 mg/kg Endosulfan maximal belastet sein müsste, um diesen ADI zu erreichen.
Von 324 zwischen 2006 und 2011 getesteten norwegischen Lachsen aus der Aquakultur z. B. überschritt keiner den Grenzwert von 0,1 mg/kg. Die meisten getesteten Tiere wiesen keinerlei Belastungen auf (Konzentrationen unterhalb der Nachweisgrenze). Die höchste überhaupt gemessene Konzentration in einer Probe lag bei 6 µg/kg α-Endosulfan und damit mehr als 16-fach niedriger als der zulässige Grenzwert (der Mittelwert aller analysierten Proben war mit 0,2 µg/kg 500-mal kleiner als der Grenzwert und damit nahe der Nachweisgrenze).
Erfreulicherweise wurden auch in den im Rahmen des Nationalen Rückstandskontrollplans durchgeführten Analysen (Bundesamt für Verbraucherschutz und Lebensmittelsicherheit – Schnellwarnungen RASFF: Lebensmittelsicherheit/Meldungen gesamt 2006 – 2014) in den letzten Jahren keine Spuren von Endosulfan in Produkten aus der Aquakultur gefunden (EC RASFF Portal). Obst, Gemüse und Gewürze dagegen werden immer noch sporadisch beanstandet.
Eine potentielle Gefährdung des Verbrauchers durch Endosulfan in Fisch und Krebstieren ist daher wohl als sehr gering einzustufen.
Amaraneni, S.R., 2002. Persistence of pesticides in water, sediment and fish from fish farms in Kolleru Lake, India. Journal of the Science of Food and Agriculture 82, 918-923.
Berntssen, M.H.G., Glover, C.N., Robb, D.H.F., Jakobsen, J.V., Petri, D., 2008. Accumulation and elimination kinetics of dietary endosulfan in Atlantic salmon (Salmo salar). Aquatic Toxicology 86, 104-111.
Casida, J.E., 1993. Insecticide action at the GABA-gated chloride channel – recognition, progress, and prospects. Archives of Insect Biochemistry and Physiology 22, 13-23.
Da Cuna, R.H., Pandolfi, M., Genovese, G., Piazza, Y., Ansaldo, M., Lo Nostro, F.L., 2013. Endocrine disruptive potential of endosulfan on the reproductive axis of Cichlasoma dimerus (Perciformes, Cichlidae). Aquatic Toxicology 126, 299-305.
Desalegn, B., Takasuga, T., Harada, K.H., Hitomi, T., Fujii, Y., Yang, H.R., Wang, P.Y., Senevirathna, S., Koizumi, A., 2011. Historical trends in human dietary intakes of endosulfan and toxaphene in China, Korea and Japan. Chemosphere 83, 1398-1405.
Easton, M.D.L., Luszniak, D., Von der Geest, E., 2002. Preliminary examination of contaminant loadings in farmed salmon, wild salmon and commercial salmon feed. Chemosphere 46, 1053-1074.
EFSA Panel on Contaminants in the Food Chain (CONTAM); Scientific Opinion on the toxicity of endosulfan in fish. EFSA Journal 2011;9(4):2131.
Fang, Y.Y., Nie, Z.Q., Yang, Y.M., Die, Q.Q., Liu, F., He, J., Huang, Q.F., 2015. Human health risk assessment of pesticide residues in market-sold vegetables and fish in a northern metropolis of China. Environmental Science and Pollution Research 22, 6135-6143.
Gebbink, W.A., Berger, U., Cousins, I.T., 2015. Estimating human exposure to PFOS isomers and PFCA homologues: The relative importance of direct and indirect (precursor) exposure. Environment International 74, 160-169.
Naqvi, S.M., Vaishnavi, C., 1993. Bioacculuative potential and toxicity of Endosulfan insecticide to nontarget animals. Comparative Biochemistry and Physiology C-Pharmacology Toxicology [&] Endocrinology 105, 347-361.
Nøstbakken, O.J., Hove, H.T., Duinker, A., Lundebye, A.-K., Berntssen, M.H.G., Hannisdal, R., Lunestad, B.T., Maage, A., Madsen, L., Torstensen, B.E., Julshamn, K., 2015. Contaminant levels in Norwegian farmed Atlantic salmon (Salmo salar) in the 13-year period from 1999 to 2011. Environment International 74, 274-280.
Nowak, B., Goodsell, A., Julli, M., 1995. Residues of Endosulfan in carp as an indicator of exposure conditions. Ecotoxicology 4, 363-371.
Peterson, S.M., Batley, G.E., 1993. The fate of Endosulfan in aquatic ecosystems. Environmental Pollution 82, 143-152.
RASFF Portal der Europäischen Kommission. [Suchbegriff „Endosulfan“, 09.05.2019] https://webgate.ec.europa.eu/rasff-window/portal/
Ratra, G.S., Kamita, S.G., Casida, J.E., 2001. Role of human GABA(A) receptor beta 3 subunit in insecticide toxicity. Toxicology and Applied Pharmacology 172, 233-240.
Ruzzin, J., Bethune, C., Goksøyr, A., Hylland, K., Lee, D.H., Jacobs Jr, D.R., Carpenter, D.O., 2015. Comment on "Contaminant levels in Norwegian farmed Atlantic salmon (Salmo salar) in the 13-year period from 1999 to 2011" by Nøstbakken et al. Environment International 80, 98-99.
Silva, E., Daam, M.A., Cerejeira, M.J., 2015. Predicting the aquatic risk of realistic pesticide mixtures to species assemblages in Portuguese river basins. Journal of Environmental Sciences-China 31, 12-20.
Silva, M.H., Gammon, D., 2009. An Assessment of the Developmental, Reproductive, and Neurotoxicity of Endosulfan. Birth Defects Research Part B-Developmental and Reproductive Toxicology 86, 1-28.
Wang, D.-G., Alaee, M., Guo, M.-X., Pei, W., Wu, Q., 2014. Concentration, distribution, and human health risk assessment of endosulfan from a manufacturing facility in Huai'an, China. Science of the Total Environment 491, 163-169.
Weber, J., Halsall, C.J., Muir, D., Teixeira, C., Small, J., Solomon, K., Hermanson, M., Hung, H., Bidleman, T., 2010. Endosulfan, a global pesticide: A review of its fate in the environment and occurrence in the Arctic. Science of the Total Environment 408, 2966-2984.
Xia, T., Nitschke, M., Zhang, Y., Shah, P., Crabb, S., Hansen, A., 2015. Traffic-related air pollution and health co-benefits of alternative transport in Adelaide, South Australia. Environment International 74, 281-290.
[Stand 05/2019]

