Eingerolltes, für den Menschen infektiöses Larven von Anisakis pegreffii an der Leber eines paratenischen Wirts (Blauer Wittling, Micromesistius poutassou).
Foto: Tina Pavelin, Institute of Oceanography and Fisheries, Split
Auf einen Blick: Parasitäre Zoonosen
Man kann davon ausgehen, dass nahezu alle wild gefangenen Fische von Parasiten befallen sind. Das ist natürlich und bei einem geringen oder moderaten Befall werden die Fische auch keine Anzeichen einer Krankheit zeigen. Für den Verzehr der Fische sind die allermeisten Fischparasiten völlig unproblematisch, weil sie den Menschen nicht infizieren können. Es gibt jedoch sowohl im Süß- als auch im Meerwasser verschiedene Parasiten, die von Fischen auf den Menschen übertragen werden können, und die teilweise schwerwiegende Erkrankungen verursachen. Bei diesen parasitären Zoonosen handelt es sich um Infektionen mit bestimmten Saugwürmern (Trematoden), Bandwürmern und Fadenwürmern (Nematoden). Ob Fische aus der Aquakultur ein Infektionsrisiko für den Menschen darstellen, hängt entscheidend davon ab, wie effektiv die komplexen Entwicklungszyklen der Parasiten durch die Produktionsmethoden unterbrochen oder unter Umständen auch befördert werden. Bei der Produktion von Fischen unter hohen Hygienestandards in geschlossenen Systemen wie Kreislaufanlagen kann die Übertragung parasitärer Zoonosen ausgeschlossen werden.
Dieser Artikel enthält umfangreiche Informationen zu den Entwicklungszyklen, der Verbreitung und der medizinischen Bedeutung der weltweit wichtigsten durch Fische übertragenen parasitären Zoonoseerreger.
Der Infektionsweg vom Fisch zum Menschen
Alle von Fischen auf den Menschen übertragbaren Parasiten haben komplexe Entwicklungszyklen. Das heißt, sie benötigen in ihrem Lebenszyklus einen oder mehrere Zwischenwirte (Wasserschnecken oder Kleinkrebse), um sich zu entwickeln und letztendlich einen Endwirt zu infizieren. In allen hier besprochenen Fällen ist der Fisch Zwischenwirt oder Stapelwirt (paratenischer Wirt) für den Parasiten. Der Mensch ist Endwirt oder Fehlwirt und kann sich demzufolge nur infizieren, wenn er lebende infektiöse Larven der Parasiten aufnimmt. Dies geschieht durch Verzehr von Fischprodukten mit lebenden Parasitenlarven, also von rohem, nur unzureichend durchgegartem, unzureichend mariniertem oder kalt geräuchertem Fisch. Das Risiko, sich beim Genuss von Fisch mit einem parasitischen Wurm zu infizieren, hängt also nicht nur mit der Verbreitung der Parasiten, sondern auch mit traditionellen und neu aufkommenden Essgewohnheiten zusammen.
Die zunehmende Popularität von Sushi, Sashimi, Ceviche und Carpaccio hat das Risiko einer Infektion in den Ländern erhöht, in denen roher Fisch nicht zur traditionellen Küche gehört. Um dieses Risiko auszuschalten, regelt die EU-Verordnung (EG) 853/2004 Folgendes: Fischereierzeugnisse, die für den Rohverzehr oder andere Zubereitungsarten bestimmt sind, bei denen die Parasiten nicht abgetötet werden, müssen mindestens 24 Stunden bei mindestens –20 °C eingefroren werden. Neben dem Rohverzehr, wie bei der Zubereitung von Sushi, umfasst die Verordnung das Kalträuchern (Kerntemperatur steigt nicht über 60 °C) von Hering, Makrele, Sprotte und Wildlachs sowie das Marinieren und Salzen, sofern dies nicht ausreicht, um Parasiten abzutöten. Ausnahmeregelungen sind möglich, wenn epidemiologische Daten zeigen, dass von Fischen einer bestimmten Herkunft keine Gesundheitsgefahr ausgeht. Fischerzeugnisse, bei denen mit bloßem Auge Parasiten erkennbar sind, dürfen nicht zum menschlichen Verzehr abgegeben werden. In der Schweiz regelt eine ähnliche Verordnung das Risiko von durch Fische übertragenen Zoonosen (Hygieneverordnung EDI, 817.024.1). Bemerkenswert ist, dass die Larven von Saugwürmern (Metazerkarien) bei dieser vorgeschriebenen Behandlung nicht in jedem Fall sicher abgetötet werden. Sicher ist immer ein gründliches Erhitzen von Fischprodukten. Für den Rohverzehr sollten an der Fischtheke nur Fischprodukte ausgewählt werden, die entsprechend gekennzeichnet sind.

Abbildung: Für den Menschen infektiöses Larvenstadium (Plerozerkoid) des Bandwurms Dibothriocephalus latus in der Muskulatur eines Europäischen Flussbarschs (Perca fluviatilis). Foto: Roman Kuchta, Czech Academy of Sciences, České Budějovice
Infektion mit Saugwürmern (Trematoda)
Alle von Fischen auf den Menschen übertragbaren Saugwürmer sind sich in ihren Entwicklungszyklen und Übertragungswegen sehr ähnlich. Die Parasiten haben einen komplexen Entwicklungszyklus mit zwei Zwischenwirten und einem Endwirt, in dem sie geschlechtsreif werden. Das aus dem Ei schlüpfende erste Larvenstadium (Miracidium) entwickelt sich in einer Wasserschnecke zu freischwimmenden Zerkarien, die einen Fisch infizieren. Dort entwickeln sich die für den Endwirt und damit auch Menschen infektiösen Larven (Metazerkarien).
Die Metazerkarien von Leberegeln (Opisthorchiidae) finden sich eingekapselt meist im Muskel oder in der Unterhaut der Fische und sind je nach Art etwa 0,13 bis 0,20 mm groß. Beim Endwirt, also auch beim Menschen, leben die 6 bis 12 mm großen, lanzettlich-blattförmigen adulten Würmer in den Gallengängen. Pathologische Veränderungen infolge einer Infektion mit Leberegeln betreffen die Gallengänge, Leber, Gallenblase und Bauchspeicheldrüse. Chronische Infektionen mit einer hohen Wurmlast führen im Laufe mehrerer Jahre zu langsam fortschreitenden, schweren Krankheitsverläufen bis hin zum Tod. Es kommt zu einer Erweiterung, Verdickung und Entzündung der Gallengänge und letztendlich zu Gallengangkarzinomen. Klinischen Symptome äußern sich als allgemeines Unwohlsein, leichtes Fieber, Gelbsucht, Unterleibsbeschwerden und Verdauungsstörungen. Leichte Infektionen verlaufen oft asymptomatisch. Eine Behandlung ist mit Praziquantel möglich.
Der Katzenleberegel Opisthorchis felineus kommt in weiten Teilen Europas (außer Großbritannien, Irland, Finnland und Skandinavien), Kasachstans und Russlands östlich bis Sibirien vor. Als Zwischenwirt für O. felineus dienen viele, überwiegend cyprinide Fischarten (Karpfenartige). Die wichtigsten Quellen für Infektionen beim Menschen sind die Orfe und die Brachse (oft auch Brasse genannt). Endwirte von O. felineus sind gewöhnlich Katzen, Hunde, Füchse und Schweine, aber auch etliche andere fischfressende Säugetiere. Bei Füchsen im Stadtgebiet Berlin wurde Ende der 1990er Jahre serologisch eine Prävalenz von O. felineus von fast 50 % nachgewiesen.
Die Häufigkeit der Infektionen mit O. felineus beim Menschen wurde vor einigen Jahren auf 1,2 bis 1,6 Millionen Fälle geschätzt, wobei die bei Weitem meisten Fälle in Russland im Einzugsgebiet des Ob in Westsibirien zu beobachten sind. Erkrankungen mit durch Fische übertragenen Saugwürmern spielen in Ostasien und Südostasien eine deutlich größere Rolle als in Europa und sind dort ein großes Gesundheitsproblem. Dies hängt ursächlich damit zusammen, dass in diesen Regionen gerne roher Süßwasserfisch verzehrt wird. In der EU wurde in den letzten 50 Jahren in Deutschland, Griechenland und Italien von Infektionen des Menschen berichtet. Die Fälle in Italien konnten alle auf den Verzehr roher Filets von der Schleie zurückgeführt werden.
Deutlich häufiger sind Infektionen des Menschen mit Opisthorchis viverrini oder Clonorchis sinensis. Neuere Schätzungen gehen davon aus, dass 16 bis 44 Millionen Menschen mit diesen Leberegeln infiziert sind. Opisthorchis viverrini ist in Südostasien beheimatet. Der Verbreitungsschwerpunkt liegt im Nordosten Thailands, in Laos, in Kambodscha und im südlichen Vietnam. Endwirte des Parasiten sind fischfressende Säugetiere, wie die Fischkatze. Wichtige zweite Zwischenwirte sind Cypriniden (Karpfenartige). Die Infektion des Menschen erfolgt auch hier durch den Konsum von rohem Fisch. Speziell im nördlichen Thailand ist die hohe Prävalenz bei Menschen ein großes medizinisches Problem.
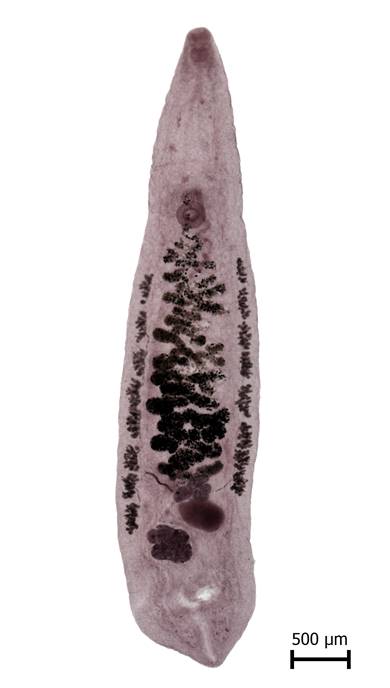
Abbildung: Der Leberegel Opisthorchis viverrini ist in Südostasien beheimatet. Der Parasit befällt die Gallengänge von fischfressenden Säugetieren und des Menschen. Foto: Roman Kuchta, Czech Academy of Sciences, České Budějovice
Clonorchis sinensis ist in China (außer im Nordwesten), angrenzenden Gebieten im Osten Russlands, Taiwan, Südkorea und im nördlichen Vietnam verbreitet. Infektionen in Hongkong werden auf importierten Fisch aus China zurückgeführt. Zwischenwirt für C. sinensis sind viele Süßwasserfische, insbesondere Cypriniden. Endwirte sind Katzen, Hunde, Schweine und Ratten. Infektionsquelle für den Menschen sind Fischarten, die roh verzehrt werden, wie zum Beispiel Graskarpfen, Silberkarpfen und Schwarzer Armur. Im südlichen China ist es traditionelle Praxis, Karpfenteiche mit menschlichen Fäkalien zu düngen. Dies hat zur Folge, dass die Eier von C. sinensis zu den Zwischenwirten gelangen und so der Entwicklungszyklus des Parasiten geschlossen bleibt.
Ein weiterer durch Fische übertragener Leberegel ist Metorchis conjunctus in Nordamerika. Seltene Infektionen des Menschen werden aus Kanada berichtet.
Neben den durch Fische übertragenen Leberegeln gibt es durch Süß- oder Brackwasserfische übertragene Saugwürmer, die beim Endwirt im Darm leben. Endwirte sind fischfressende Vögel und Säugetiere. Etliche Arten aus den Familien Heterophyidae und Echinostomatidae können auch den Menschen infizieren. Infektionen beim Menschen treten in weiten Teilen Asiens und an der Pazifikküste Nordamerikas auf, wo sie lokal hohe Prävalenzen erreichen können. Im nördlichen Nildelta sind Infektionen des Menschen mit Heterophyes heterophyes weit verbreitet, was mit dem Konsum von unzureichend zubereiteten Meeräschen in Verbindung gebracht wird. Die klinische Bedeutung der meist nur wenige Millimeter großen, im Dünndarm lebenden adulten Parasiten ist im Vergleich zu einer Infektion mit Leberegeln im Allgemeinen gering. Geringe Infektionen verlaufen oft symptomlos oder mit milden Darmproblemen, bei starken Infektionen kann es zu Unterleibskrämpfen und Gewichtsverlust kommen. Eine Saugwurminfektion des Darms kann, wie die Infektion mit Leberegeln, mit Praziquantel behandelt werden.
Infektion mit Bandwürmern (Cestoda)
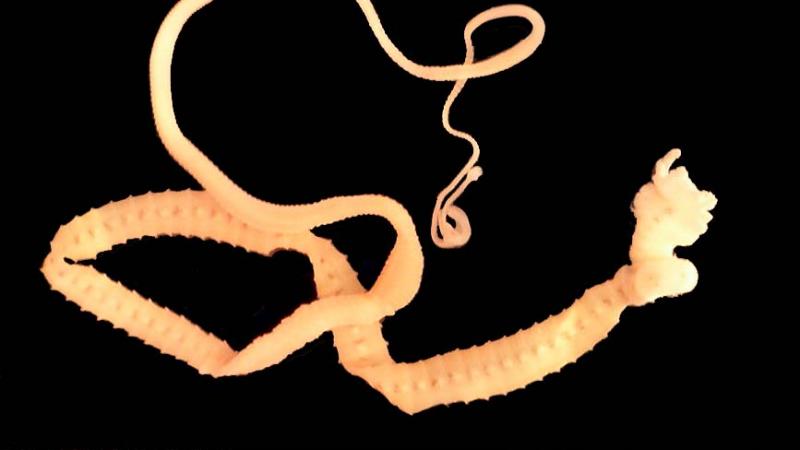
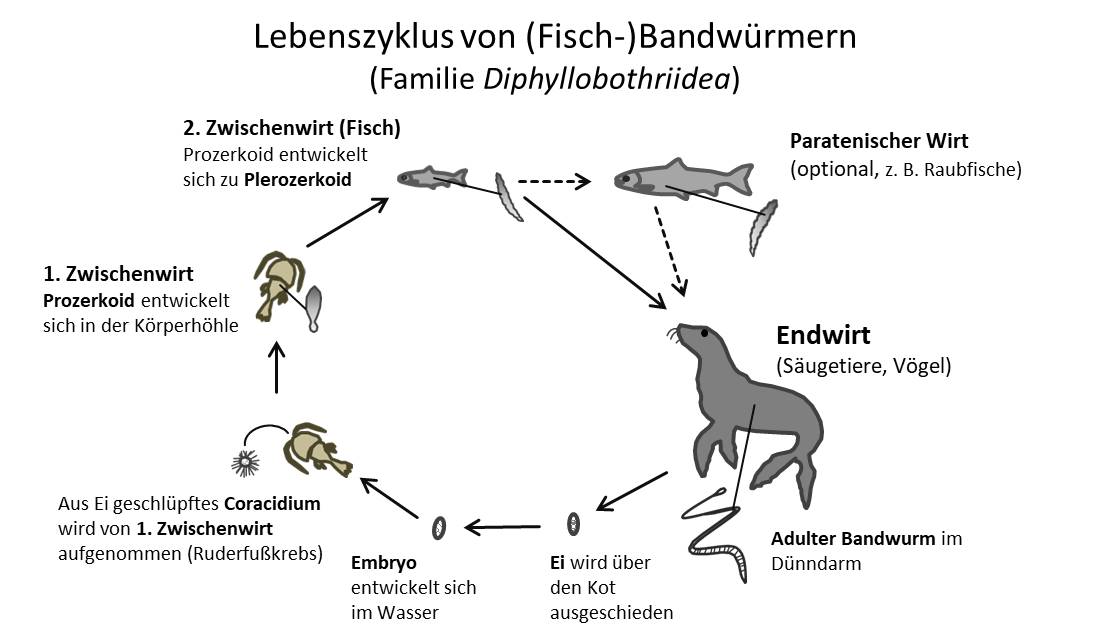
Bandwürmer der Familie Diphyllobothriidea sind Darmparasiten fischfressender Vögel und Säugetiere. Sie haben einen komplexen Entwicklungszyklus mit Hüpferlingen (Ruderfußkrebsen) als erstem Zwischenwirt und Fischen als zweitem Zwischenwirt. Darüber hinaus können Fische als Stapelwirte fungieren. Im Fisch entwickelt sich das für den Endwirt infektiöse Larvenstadium. Dieses Plerozerkoid ist wenige Millimeter groß und findet sich abhängig von der Art meist frei, selten eingekapselt, in der Muskulatur, den inneren Organen oder der Leibeshöhle. Endwirte sind fischfressende Vögel und Säugetiere. Von etwa 50 bekannten Arten, die früher der Gattung Diphyllobothrium zugeordnet wurden, sind für 14 Arten Infektionen beim Menschen beschrieben. Da die Infektion durch Verzehr vom rohem oder nicht ausreichend erhitztem Fisch erfolgt, werden diese Bandwürmer auch als Fischbandwürmer bezeichnet. Mit einer Länge von bis zu 20 m sind dies die längsten Parasiten, die den Menschen befallen können. Die bei Weitem häufigsten für den Menschen infektiösen Arten sind Dibothriocephalus latus und mit einem deutlich geringeren Anteil Dibothriocephalus nihonkaiense und Adenocephalus pacificus. Es wird geschätzt, dass weltweit bis zu 20 Millionen Menschen mit Fischbandwürmern infiziert sind.

Abbildung: Für den Menschen infektiöses Larvenstadium (Plerozerkoid) von Dibothriocephalus latus. Endwirte des Bandwurms sind fischfressende Vögel und Säugetiere. Foto: Roman Kuchta, Czech Academy of Sciences, České Budějovice
Im Menschen haften sich die Fischbandwürmer im hinteren Bereich des Dünndarms (Ileum) an und reifen innerhalb von 2 bis 6 Wochen zum adulten Wurm heran. Trotz der Größe der Parasiten verlaufen viele Infektionen asymptomatisch. In etwa 20 % der Fälle kommt es zu Unterleibsschmerzen, Durchfall oder Verstopfung. Selten kann eine durch Vitamin B12 Mangel verursachte Anämie auftreten. Andere schwerwiegende Komplikationen sind sehr selten. Zur Therapie werden Praziquantel oder Niclosamid verwendet. Diese Medikamente töten den Fischbandwurm schnell ab.
D. latus ist circumpolar verbreitet. Das Plerozerkoid von D. latus findet sich meist nicht eingekapselt in der Muskulatur von Süßwasserfischen, meist Flussbarsch, Hecht und Quappe. Bei als D. latus bestimmten Plerozerkoiden in Salmoniden und Coregonen handelt es sich wahrscheinlich um andere Arten. Endwirte von D. latus sind neben dem Menschen fischfressende Säugetiere wie Hunde, Marderhunde und Füchse. In Europa sind die Fallzahlen von humanen Infektionen in den historisch stark betroffenen baltischen Staaten, Polen, Rumänien, Schweden, Norwegen und Finnland stark rückläufig. Stattdessen traten in den letzten Jahrzehnten vermehrt Fälle um die großen subalpinen Seen in der Schweiz, Italien und Frankreich auf, die mit dem Konsum von rohem oder nicht ausreichend erhitztem Flussbarsch zu erklären sind. Die Infektionsrate bei Barschen im Lago Maggiore lag zwischen 2005 und 2008 bei 14 %. Neuere molekularbiologische Untersuchungen legen nahe, dass es sich nicht bei allen als D. latus bestimmten Fischbandwürmern tatsächlich um diese Art handelt. Wahrscheinlich spielen auch andere Dibothriocephalus-Arten wie D. dendriticus bei Infektionen des Menschen eine größere Rolle als bisher angenommen. Wichtigste zweite Zwischenwirte für D. dendriticus sind Salmoniden und Coregonen.
Dibothriocephalus nihonkaiense ist in an den asiatischen (Russisch-Fernost, Japan, China, Korea) und amerikanischen Küsten des nördlichen Pazifiks verbreitet. Zweite Zwischenwirte sind verschiedene pazifische Lachsarten, Huchen und seltener Saiblinge, bei denen die Plerozerkoide frei oder eingekapselt im Muskelgewebe liegen. Die von der Pazifikküste Südamerikas berichteten Infektionen gehen nahezu ausschließlich auf die dort heimische Art Adenocephalus pacificus zurück, deren Plerozerkoide in der Muskulatur verschiedener Meeresfische gefunden werden. Eine Übertragung von Fischbandwürmern auf Menschen durch Salmoniden aus Zuchtbetrieben wird als unwahrscheinlich eingeschätzt.
Infektion mit Fadenwürmern (Nematoda)
Erkrankungen durch von Fischen auf Menschen übertragene Fadenwürmer werden meist durch Vertreter der Gattungen Anisakis (siehe Titelbild) und, in geringerem Umfang, Pseudoterranova und Contracaecum verursacht. Molekularbiologische Untersuchungen zeigten, dass es in den Gattungen Anisakis spp. und Pseudoterranova spp. mehrere Schwesternarten mit unterschiedlicher geographischer Verbreitung und unterschiedlichem Wirtsspektrum gibt. Diese Arten mit ausschließlich marinen Entwicklungszyklen benötigen planktonische Krebstiere (Krill) als Zwischenwirte. Fische und Tintenfische fungieren im Entwicklungszyklus als Stapelwirte und können eine hohe Zahl an Wurmlarven akkumulieren. Adulte Anisakis spp. sind Darmparasiten bei Walen, Pseudoterranova spp. bei Seehunden, Seelöwen und Walrossen und Contracaecum spp., abhängig von der Art, ebenfalls bei marinen Säugetieren und fischfressenden Vögeln. Ob Contracaecum-Arten, die Vögeln als Endwirt nutzen, humanpathogen sein können, ist nicht bekannt. Der Mensch ist in allen Fällen ein Fehlwirt, in dem sich die Parasiten nicht zum adulten Wurm entwickeln können.
Infektionen des Menschen mit anisakiden Nematoden sind weltweit vor allem in Nordasien und Westeuropa verbreitet, aber vergleichsweise selten. Bis zum Jahr 2010 wurden lediglich 20.000 Fälle bekannt, mehr als 90 % davon aus Japan. In den letzten Jahrzehnten war allerdings ein deutlicher Anstieg der Fallzahlen zu beobachten, was sowohl mit einer verbesserten Diagnostik (Endoskopie) als auch veränderten Ernährungsgewohnheiten zusammenhängen kann. Die höchste Inzidenz von Anisakiasis in Europa hat Spanien, wo die Infektion hauptsächlich durch marinierte Anchovis erfolgt. Epidemiologisch bedeutend ist, wo im Gewebe sich die infektiösen Larven befinden. Dies hängt nicht nur davon ab, um welche Parasitenart und welchen Wirt es sich handelt, sondern auch davon, wie der Fisch nach dem Fang behandelt wird. Es wurde gezeigt, dass die Wurmlarven nach dem Tod des paratenischen Wirtes von dessen Eingeweiden in die Muskulatur wandern. Anisakis-Larven sind etwa 2 bis 3 cm lang und spiralig aufgerollt, während Pseudoterranova-Larven etwas länger und nicht derart aufgerollt sind. Die Prävalenz von anisakiden Larven in Meeresfischen kann extrem hoch sein, während bei der Untersuchung von in Europa produzierten Lachsen aus Aquakultur keine dieser Parasiten gefunden wurden.
Die klinische Symptomatik einer Anisakiasis beim Menschen hängt davon ab, wie sich die Wurmlarve nach Aufnahme im Magendarmtrakt verhält. Wird das Gewebe nicht penetriert, kann die Infektion asymptomatisch bleiben und die Würmer werden wieder ausgeschieden. Wird die Magen- oder Darmschleimhaut penetriert, treten nach einigen Stunden bzw. Tagen zusammen mit Übelkeit und Erbrechen starke Schmerzen auf. Darüber hinaus kann Anisakis beim Menschen eine starke allergische Reaktion auslösen. Bedeutsam ist, dass die hierfür verantwortlichen Allergene gegenüber Hitze und Gefrieren sehr widerstandfähig sind. Das heißt, auch wenn der Fisch oder Tintenfisch in einer Weise zubereitet wird, dass die Parasiten sicher abgetötet sind, kann es nach der Mahlzeit zu heftigen Unverträglichkeitsreaktionen kommen. Behandelt wird die Anisakiasis durch endoskopische oder chirurgische Entfernung der lebenden Parasiten.
Angot, V., Brasseur, P., 1993. European farmed Atlantic salmon (Salmo salar L.) are safe from anisakid larvae. Aquaculture, 118: 339-344.
Audicana, M.T., Ansotegui, I.J., de Corres, L.F., Kennedy, M.W., 2002. Anisakis simplex: Dangerous - Dead and alive? Trends in Parasitology 18: 20-25.
Bao, M., Pierce, G.J., Pascual, S., González-Muñoz, M., Mattiucci, S., Mladineo, I., Cipriani, P., Bušelić, I., Strachan, N.J.C., 2017. Assessing the risk of an emerging zoonosis of worldwide concern: anisakiasis. Scientific Reports 7:43699.
Bilska-Zając, E., Różycki, M., Chmurzyńska, E., Karamon, J., Sroka, J., Kochanowski, M., Kusyk, P., Cencek, T., 2015. Parasites of Anisakidae Family—Geographical Distribution and Threat to Human Health. Journal of Agricultural Science and Technology A 5: 146-152.
Chai, J.-Y., Murrell, K.D., Lymbery, A.J., 2005. Fish-borne parasitic zoonoses: Status and issues. Int J Parasitol 35: 1233-1254. doi:10.1016/j.ijpara.2005.07.013
Fan, P.C., 1998. Viability of metacercariae of Clonorchis sinensis in frozen or salted freshwater fish. International Journal for Parasitology 28: 603-605.
Huss, H.H., Embarek, P.K.B., 2003. Parasites. In: Huss, H.H., Ababouch, L., Gram, L.: Assessment and management of seafood safety and quality. FAO Fisheries Technical Paper. No. 444. Rome, FAO, 230p.
Kuchta, R., Brabec, J., Kubáčková, P., Scholz, T., 2013. Tapeworm Diphyllobothrium dendriticum (Cestoda) - Neglected or Emerging Human Parasite? PLOS 7: e2535.
Lunestad, B.T., 2003. Absence of Nematodes in Farmed Atlantic Salmon (Salmo salar L.) in Norway. Journal of Food Protection 66: 122-124.
Shamsi, S., 2019. Parasite loss or parasite gain? Story of Contracaecum nematodes in antipodean waters. Parasite Epidemiology and Control 4: e00087.
Sithithaworn, P., Andrews, R., Shekhovtsov, S.V., Mordvinov, V.A., Furman, D.P., 2014. Opisthorchis viverrini and Opisthorchis felineus. Encyclopedia of Food Safety 2: 170-178.
Scholz, T., Garcia, H., Kuchta, R., Wicht, B., 2009. Update on the Human Broad Tapeworm (Genus Diphyllobothrium), Including Clinical Relevance. Clinical Microbiology Reviews 22: 146-160.
Scholz, T., Kuchta, R., 2016. Fish-borne, zoonotic cestodes (Diphyllobothrium and relatives) in cold climates: A never-ending story of neglected and(re)-emergent parasites. Food and Waterborne Parasitology 4; 23-38.
Schuster, R., Gregor, B., Heidrich, J., Nöcler, K., Kyule, M., Wittstatt, U., 2003. A sero-epidemiological survey on the occurrence of opisthorchiid liver flukes in red foxes (Vulpes vulpes) in Berlin, Germany. Parasitol Res 90: 400–404.
Wicht, B., Limoni, C., Peduzzi, R., Petrini, O., 2009. Diphyllobothrium latum (Cestoda: Diphyllobothriidea) in perch (Perca fluviatilis) in three sub-alpine lakes: Influence of biotic and abiotic factors on prevalence. Journal of Limnology 68:167-173.
[Stand 08/2021]